宫颈癌和HPV病毒
宫颈癌是最常见的妇科恶性肿瘤之一,全世界每年约有50万宫颈癌新发病例,每年约有23万女性死于宫颈癌。在不同地区、不同经济状况的国家,宫颈癌的发病率和死亡率有着显著的差别,其中80%的病例发生在发展中国家。我国每年约有15万宫颈癌新发病例,每年约有8万人死于宫颈癌,其死亡率居妇科肿瘤的第二位。近年来,宫颈癌新发病例数在逐渐上升,并呈年轻化的趋势。
经过大量流行病学和病毒学研究证实,宫颈组织发生癌前病变直至发展为浸润性癌症与高危型人乳头瘤病毒(HPV)的持续感染有关。HPV病毒属于乳头多瘤空泡病毒科病毒属,是一种小型、无外包膜的环状DNA病毒。HPV感染主要是上皮组织,具有高度的宿主特异性,对人体特异部位的上皮细胞具有亲和力。在已发现的120多种HPV基因型中,有14种亚型(16、18、31、33、35、39、45、51、52、56、58、59、66和68)在大多数宫颈癌中会出现,被认为是高危致癌风险的亚型,简称“高危型”。
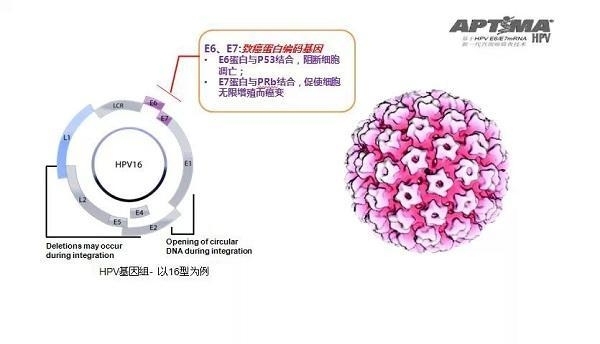
E6、E7基因的致癌机理
环状HPV基因组包括两类编码基因区,即七个早期区(E1、E2、E4、E5、E6、E7和E8)基因和两个晚期区(L1和L2)。L1和L2编码病毒衣壳蛋白,在病毒颗粒自我组装以及侵入目标细胞时起协调和识别作用。而早期区(E区)编码蛋白基因中,由E6和E7基因编码的致癌蛋白是导致宫颈上皮癌变的重要因子,这两种蛋白通过抑制两种主要抑癌蛋白p53和视网膜母细胞瘤蛋白(pRb)使被感染的细胞可无限增殖并恶性转变。p53的主要作用是发现DNA持续损伤时激活DNA修复蛋白,抑制细胞生长,当DNA损伤无法修复时会加速细胞凋亡,E6致癌基因过度表达的蛋白抵消了p53的多种抑癌作用,允许出现DNA损伤的细胞能够继续分裂。pRb作为一种抑癌蛋白,则通过调控细胞周期避免细胞过度生长,E7致癌基因表达的蛋白与pRB蛋白结合,导致蛋白降解和与pRb结合的E2F转录因子的释放。这些游离的E2F转录因子会激活许多参与在G1/S期调控点的细胞周期调控基因。这种联合效应使得存在未修复DNA损伤的细胞可以无限增殖并且保持过度增殖状态。
低危型HPV E6/E7蛋白在阻碍p53和pRb功能方面不如高危型的E6/E7蛋白强烈。从而,低危型HPV感染仅与良性增生相关,如,尖锐湿疣和易消退的低级别上皮内瘤变。
E6、E7 mRNA: 新的高危型HPV检查标志物
E6、E7基因表达癌蛋白,DNA需要首先被激活,转录大量的E6、E7 mRNA,然后再由mRNA 翻译成相应的癌蛋白。所以E6、E7 mRNA 的大量表达是细胞发生高级别病变的一个信号。作为一个新的生物标记,相比DNA,E6、E7 mRNA与“病变”的相关性更好,也越来越受到各方的关注。美国FDA已于2012年批准了全球第一个基于E6、E7 mRNA 的高危型HPV检测试剂盒 – Aptima HPV。
本文由豪洛捷提供
 李文华的博客
李文华的博客